
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
BABIO asigură autorizarea FDA 510(k) din S.U.A. pentru kitul său de transport viruși (neinactivator)
BABIO asigură autorizarea FDA 510(k) din S.U.A. pentru kitul său de transport viruși (neinactivator)
Jinan, China – octombrie 2025 – Jinan Babio Biotechnology Co., Ltd. (BABIO)anunță cu mândrie că esteKit de transport Babio® Virus (neinactivator)a primit oficialAutorizare FDA 510(k) (K250205). Această certificare marchează o piatră de hotar semnificativă pentru BABIO, reafirmând angajamentul său față de calitatea globală, siguranță și inovație în diagnosticarea clinică și sistemele de transport microbiologic.
Autorizația FDA 510(k) autorizează Kitul de transport al virusului Babio® casubstanțial echivalentla dispozitivele comercializate legal în Statele Unite, validând conformitatea acesteia cu standardele de reglementare din SUA pentru dispozitivele medicale. Această realizare demonstrează capacitățile puternice de cercetare și dezvoltare ale BABIO și excelența în producție, consolidându-și în continuare competitivitatea globală înpiata transportului virusului si colectarii specimenelor.
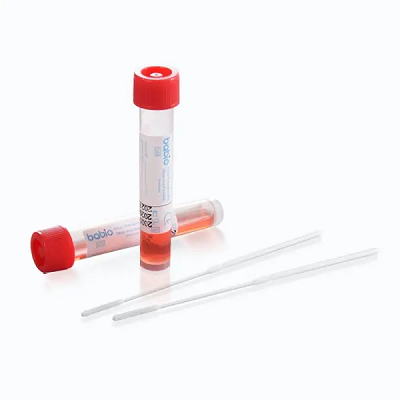
TheKit de transport Babio® Virus (neinactivator)este conceput pentru colectarea și transportul în siguranță a probelor clinice care conțin viruși. Menține integritatea probei pentru testele din aval, cum ar fiRT-PCR, cultura virala, șidiagnostic molecular, făcându-l potrivit pentru spitale, laboratoare și instituții de sănătate publică din întreaga lume.

BABIO, toproducător chinez de topde reactivi de diagnostic, medii de transport și medii de cultură, continuă să-și extindă prezența înEuropa, Statele Unite, Africa și Asia de Sud-Est, oferind soluții de încredere care îndeplinesc standardele internaționale.
Pentru mai multe informații despre produsele certificate BABIO și inovațiile de diagnosticare, vă rugăm să vizitați: https://www.babiocorp.com
#BABIO #FDA510k #VirusTransportKit #MedicalDevices #Diagnostice #BiotechChina #GlobalHealthcare #ClinicalDiagnostics #Microbiology


